Thử nghiệm hạt nano chứa axit nucleic vào điều trị ung thư não
Các nhà khoa học thuộc trường Đại học Northwestern (Mỹ) đã nghiên cứu và phát triển ra loại thuốc mới sử dụng axit nucleic hữu cơ gắn lên vật liệu nano vàng. Điều này có ý nghĩa quan trọng trong việc chữa trị ung thư và các chứng bệnh về não.
Kết quả của công trình nghiên cứu này đã được FDA (Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ) phê duyệt như một loại thuốc mới cho các thử nghiệm lâm sàng nhằm điều trị u não trên người vào tháng 1/ 2017.
Loại thuốc mới này có thể vượt qua hàng rào máu não để tiếp cận các khối u và sẽ làm tắt gen gây ung thư. Đây là một thử thách khó khăn trong điều trị các bệnh về não. Đầu năm 2017, giai đoạn 1 của dự án đã được các nhà khoa học tiến hành nhằm thử nghiệm khả năng tiếp cận của thuốc tới các khối u ở người.
Thuốc glioblastoma đại diện cho một loại thuốc mới mang tính cách mạng. Mô hình thuốc chế tạo từ các chuỗi axit nucleic hữu cơ bám trên hạt nano vàng có thể được áp dụng cho các loại bệnh thần kinh khác như Alzheimer và Parkinson, bằng cách vô hiệu hóa các gen dẫn đến những bệnh này.

Thuốc glioblastoma đại diện cho một loại thuốc mới mang tính cách mạng.
Đây là loại thuốc hiếm hoi được nghiên cứu bởi một trường đại học, không nhận tài trợ từ bất kỳ công ty dược phẩm nào nhưng lại được FDA chấp nhận đưa vào thử nghiệm lâm sàng.
Theo Jay Walsh, phó giám đốc nghiên cứu tại Đại học Northwestern: "Chúng tôi muốn đưa thuốc đến bệnh nhân càng sớm càng tốt. Hiện có nhiều bệnh nhân mắc phải căn bệnh này nhưng không có phương pháp chữa".
"Chúng tôi biết rằng loại thuốc này hoạt động trên chuột. Chúng ta cần biết liệu nó có thể vượt qua hàng rào máu-não của con người và tích tụ trong khối u của con người hay không”, Alexander Stegh, trợ lý giáo sư về thần kinh học tại Trường Y khoa Feinberg, đại học Northwestern cho biết.
Stegh đã phát triển loại thuốc này cùng Chad A. Mirkin, giáo sư trường Cao đẳng Nghệ thuật và Khoa học Weinberg và giám đốc Viện Quốc tế về Công nghệ Nano Northwestern (IIN). Ông cũng là người nắm giữ Giải thưởng Di sản công nghệ sinh học (Biotechnology Heritage Award) của nhà hóa học, sinh vật học người Mỹ George B. Rathmann.
"Nếu các hạt cầu nano vàng chứa axit nucleic vượt qua hàng rào máu não và định vị trong não, ý nghĩa của nó vượt ra khỏi việc điều trị glioblastoma, dạng ung thư não phổ biến nhất", Mirkin nói. "Điều này sẽ bổ sung khả năng điều trị các bệnh về não, bao gồm Huntington, Parkinson và Alzheimer".
Loại thuốc mới bao gồm các đoạn ngắn của RNA được sắp xếp đặc biệt trên bề mặt các hạt nano vàng hình cầu. Nó làm thay đổi cấu trúc di truyền của tế bào khối u và làm giảm khả năng phân chia của chúng. Thuốc nhắm tới mục tiêu tác động vào gene BCL2L12, loại gene có liên quan tới apoptosis, cơ chế gây chết tế bào theo chương trình.
Bệnh nhân u bướu cổ được điều trị bằng hóa trị liệu, xạ trị và phẫu thuật. Mặc dù vậy, căn bệnh này không có phương án chữa trị dứt điểm. Với 30.000 người Mỹ, sau khi được chẩn đoán mắc bệnh ung thư não, thời gian sống còn lại của họ chỉ từ 14 đến 16 tháng.

Loại thuốc mới bao gồm các đoạn ngắn của RNA được sắp xếp đặc biệt trên bề mặt các hạt nano vàng hình cầu.
Theo tiến sĩ Priya Kumthekar, trợ lý giáo sư về thần kinh học và khoa học ung thư học tại Trường Y khoa Feinberg: "Chúng tôi cần một cách điều trị hiệu quả để chữa trị căn bệnh chết người này”. Kumthekar là nhà nghiên cứu chính của cuộc thử nghiệm tại đại học Northwestern. Cô sẽ tiến hành một cuộc thử nghiệm trên 6-8 người mắc căn bệnh glioblastoma, dạng u não phổ biến nhất.
Nghiên cứu sẽ được thử nghiệm trên những người bị tái phát sau khi phẫu thuật loại bỏ khối u. Họ sẽ nhận một liều thuốc tiêm tĩnh mạch trước khi phẫu thuật. Sau khi cắt bỏ khối u, Kumthekar và nhóm của cô sẽ nghiên cứu khối u để xác định độ mạnh liều thuốc cần dùng để vượt qua hàng rào máu-não.
"Kết quả nghiên cứu trên động vật cho thấy loại thuốc này thấm sâu vào các khối u", Kumthekar nói. "Chúng tôi dự đoán trường hợp đó cũng sẽ xảy ra trên khối u của người bệnh".
Theo Tiến sĩ Frank Giles, cựu đại diện nhà tài trợ của Đại học Northwestern, "Northwestern tập trung vào việc cung cấp các liệu pháp tốt hơn để chữa trị cho bệnh nhân”. “Áp dụng kiến thức khoa học mới là cách tốt nhất để phát triển liệu pháp mới", Frank Giles cho biết. Cả Kumthekar, Stegh, Mirkin và Giles đều là thành viên của Trung tâm Ung thư Lurie.
“Đây là một quá trình phức tạp, công phu, đòi hỏi sự phối hợp chặt chẽ giữa các nhóm nghiên cứu thuộc Đại học Northwestern và Viện Y khoa Northwestern Medicine”, Ann Adams, phó giám đốc nghiên cứu tại Đại học Northwestern cho biết.
Theo tiến sĩ Leon Platanias, giám đốc Trung tâm Ung thư Lurie: "Công nghệ này thật tuyệt diệu, chúng ta có thể có những cách tiếp cận mới hiệu quả hơn để điều trị u não và các khối u khác trong tương lai".
Sự ra đời của loại thuốc mới
Stegh và Mirkin đã hợp tác từ năm 2009 để giải quyết vấn đề khó khăn trong việc phát triển các phương pháp điều trị bệnh u nang glioblastoma. Họ lần đầu tiên kết hợp với nhau thông qua Trung tâm Ung thư Đại học Northwestern.
Nhiệm vụ của Mirkin là nghiên cứu, chế tạo các axit nucleic gắn trên vật liệu nano vàng, một hình thức có dạng hình cầu mới của DNA và RNA và không độc với con người. Trong đó, chu trình axit nucleic được thiết kế để phù hợp với gen mục tiêu.
Với Stegh, nhiệm vụ của ông là nghiên cứu về gene. Vào năm 2007, ông và các đồng nghiệp đã xác định được gene BCL2L12 biểu hiện vượt trội ở khối u glioblastoma. Điều này có liên quan đến khả năng đề kháng của glioblastoma.
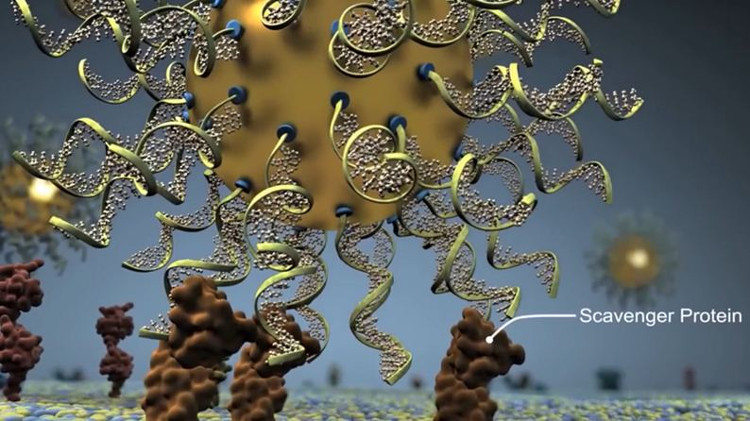
Một khi đã vào bên trong các tế bào ung thư, loại thuốc này vô hiệu hóa các gene gây bệnh.
Cơ chế hoạt động
Với tính chất đặc biệt của nano vàng, thuốc dễ dàng vượt qua hàng rào máu-não, tiến tới tiếp cận khối u não. Một khi đã vào bên trong các tế bào ung thư, loại thuốc này vô hiệu hóa các gene gây bệnh. Chu trình được lập trình của RNA hoạt động như một công tắc, nó ngăn cản các tế bào sản xuất một số loại protein cụ thể có liên quan đến bệnh. Kết quả là chúng sẽ tiêu diệt một cách có chọn lọc tế bào ung thư và làm suy giảm sự phát triển của tế bào.
Chìa khóa cho sự thành công của loại thuốc mới là nhờ cấu trúc hình cầu 3-D của vật liệu nano vàng và nồng độ axit nucleic. Axit nucleic bình thường không thể xâm nhập vào tế bào hoặc vượt qua hàng rào máu-não, thế nhưng các axit nucleic gắn trên hạt nano vàng lại hoàn toàn có thể.
Kết quả nghiên cứu trên động vật
Vào năm 2013, Mirkin và Stegh là những đồng tác giả cao cấp của một nghiên cứu về động vật được xuất bản trong tạp chí Science Translational Medicine. Nhóm nghiên cứu của họ là những người đầu tiên chứng minh việc cung cấp một loại thuốc bằng cách tiêm tĩnh mạch có khả năng vô hiệu hóa một gen gây ung thư quan trọng. Nó làm giảm sự tiến triển của khối u và tăng tỉ lệ sống sót của những con chuột mang u não glioblastoma.
Ở những con chuột mắc glioblastoma, khoảng 1% liều tiêm đã tích lũy được trong mô khối u não não. Điều tuyệt vời là khi đã vào được trong não, các axit nucleic nano vàng hình cầu này tự động tập trung tích luỹ trong mô khối u. Điều này có được là do khả năng tích tụ của các hạt nano vàng trong mô khối u theo đường dẫn của các mạch máu. Nhờ vậy, tỉ lệ sống sót của những con chuột này tăng gần 20%, kích thước khối u cũng giảm 3-4 lần so với nhóm đối chứng.
Nền tảng cấu trúc nano trong nghiên cứu này được Mirkin phát triển tại đại học Northwestern kể từ năm 1996. Đây là lần đầu tiên người ta nhận ra các cấu trúc nano được tiêm vào một cơ thể động vật có thể tự động tìm mục tiêu trong não. Điều này mang lại hiệu quả cao cho các liệu pháp điều trị. Đại học Northwestern và một số nhà nghiên cứu liên quan sẽ được hưởng lợi về mặt tài chính nhờ kết quả của nghiên cứu này.
Y học - Sức khỏe
-

Tại sao bạn dễ ngủ trên ghế sofa và sau đó tỉnh táo trên giường?
-

Dấu hiệu biển nước khổng lồ tồn tại dưới lớp vỏ Trái đất
-

Việt Nam có một loại củ phơi khô được ví như "thuốc trường thọ"
-

Vật nguy hiểm nhất thế giới: Chỉ nhìn 5 phút đã mất mạng, hàng trăm năm nữa cũng không thể đến gần!
-

Cận cảnh sinh vật bí ẩn gây chấn động Malaysia: Như một khối thịt khổng lồ đến từ hành tinh khác
-

Những bức ảnh thay đổi cái nhìn về lịch sử
Đời sống
-

Công nghệ xử lý rác không cần phân loại
-

Nhiều tuyến đê bị sạt lở, đe dọa Hà Nội
-

Thế giới mất phần rừng nhiệt đới tương đương với diện tích Đan Mạch
-

Bão Nakri gây mưa lớn, nhiều nơi mất điện
-

Glybera - Loại thuốc chữa bệnh chỉ dành cho người giàu
-

Thông tin mới nhất về cơn bão Talim và áp thấp nhiệt đới trên biển Đông