Sắp có thuốc molnupiravir "made in Việt Nam"
Bộ Y tế đang trình Ủy ban thường vụ Quốc hội, Chính phủ, dự thảo xin cơ chế cấp phép với các thuốc điều trị Covid-19; một số doanh nghiệp đã nhận chuyển giao công nghệ và nguyên liệu thuốc molnupiravir, chờ được phê duyệt sản xuất.
Một tấn nguyên liệu để bào chế 4.750.000 viên nén molnupiravir thương hiệu Movinavir 200 mg điều trị Covid-19 của Công ty Optimus Pharma (Ấn Độ), đã theo chuyên cơ đoàn công tác của Chủ tịch Quốc hội Vương Đình Huệ từ Ấn Độ về Việt Nam, hai ngày trước. Số nguyên liệu này đã được bàn giao cho Công ty cổ phần hóa - dược phẩm Mekophar, một trong những doanh nghiệp dược đầu tiên của Việt Nam đạt tiêu chuẩn GMP-WHO (tiêu chuẩn thực hành tốt sản xuất thuốc).
Đại diện Mekophar cho biết trước đó đã nộp hồ sơ và đang đợi Bộ Y tế xem xét cấp số đăng ký lưu hành thuốc Movinavir. Công ty này đã hoàn tất nhận chuyển giao công nghệ từ Ấn Độ, dự kiến khi được Bộ Y tế phê duyệt sẽ nhập thêm nguyên liệu và bắt tay ngay vào sản xuất.
Về việc này, ông Phạm Sanh Châu (Đại sứ Việt Nam tại Ấn Độ) cho biết, các công ty Việt Nam đang làm việc với Ấn Độ để nhập nguyên liệu chuẩn bị cho sản xuất khi được Bộ Y tế cấp số đăng ký. Tuy nhiên, Đại sứ không cho biết số lượng doanh nghiệp đang đàm phán mua nguyên liệu.
Molnupiravir là hoạt chất trong thuốc, có tác dụng kháng virus, đang trong giai đoạn thử nghiệm và chưa được cấp phép lưu hành tại Việt Nam. Tuy nhiên thuốc này được xem là "vũ khí" quan trọng trong điều trị F0 tại nhà, do tác dụng giảm tải lượng virus khi sử dụng ở giai đoạn đầu mắc bệnh, từ đó giảm nguy cơ trở nặng và tử vong.
Thuốc là mặt hàng đặc biệt, muốn được Bộ Y tế xét duyệt, cấp phép đăng ký lưu hành phải tốn thời gian khoảng 2-3 năm. Theo Bộ Y tế, hiện khoảng 10 công ty dược đã nộp hồ sơ để được sản xuất thuốc chứa hoạt chất molnupiravir. Tuy nhiên, Luật Dược hiện hành quy định thuốc mới đăng ký lưu hành phải có hồ sơ thử nghiệm lâm sàng, trong khi đó thuốc molnupiravir mới thử nghiệm thời gian qua trên quy mô nhỏ, chưa thể đáp ứng.
Để gỡ vướng mắc, Cục quản lý Dược cùng Vụ Pháp chế (Bộ Y tế) đã xây dựng, xin cơ chế cấp phép cho sản xuất thuốc molnupiravir. Trong dự thảo vừa trình Chính phủ, Bộ Y tế đề xuất đối với thuốc mới có chỉ định sử dụng phòng, điều trị Covid-19 sản xuất trong nước được miễn nộp hồ sơ lâm sàng nếu có cùng hoạt chất, dạng bào chế, đường dùng với thuốc có chỉ định sử dụng phòng, điều trị Covid-19 đã được một trong các cơ quan quản lý dược thuộc danh sách SRA (Cơ quan Quản lý Dược nghiêm ngặt theo Tổ chức Y tế Thế giới) cấp phép lưu hành.
"Nếu đề xuất này được thông qua thì các đơn vị có thể sản xuất thuốc chứa hoạt chất molnupiravir tại Việt Nam", một lãnh đạo Vụ Pháp chế trả lời VnExpress ngày 22/12. Bà kỳ vọng khi đó, năng lực sản xuất trong nước sẽ cơ bản đáp ứng nhu cầu thuốc kháng virus cho nhu cầu điều trị.
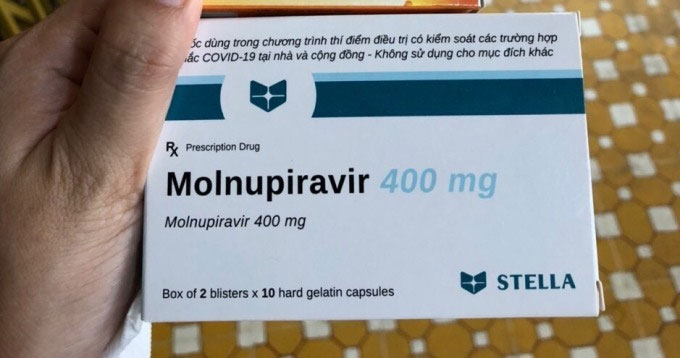
Thuốc kháng virus molnupiravir phát cho F0 khi đi cách ly tập trung. (Ảnh: Nhân vật cung cấp)
Tính đến ngày 18/12, Bộ Y tế đã phân bổ tổng cộng 300.000 liều thuốc molnupiravir cho Chương trình thí điểm điều trị có kiểm soát các trường hợp mắc Covid-19 thể nhẹ. Chương trình được triển khai tại TP HCM từ giữa tháng 8 và hiện mở rộng 46 địa phương có dịch. Trên thực tế, F0 điều trị tại nhà ở nhiều tỉnh thành đang thiếu thuốc molnupiravir.
Theo Chánh văn phòng Sở Y tế TP HCM Nguyễn Thị Huỳnh Mai, số lượng gói thuốc C được Bộ Y tế phân bổ không đủ để cấp phát rộng rãi cho tất cả người có kết quả test nhanh dương tính Covid-19, trong bối cảnh số F0 tăng. Thành phố quyết định chỉ cấp phát thuốc molnupiravir cho người có nguy cơ, cao tuổi, có bệnh nền, mà không phát cho tất cả F0.
Cơ quan Quản lý Dược phẩm và Thực phẩm Mỹ (FDA) đang xem xét các dữ liệu lâm sàng cho quyết định cấp phép lưu hành thuốc. Các quốc gia châu Á, trong đó có Ấn Độ, cũng đang rà soát dữ liệu lâm sàng đối với các thuốc được công ty phát minh là MSD nhượng quyền sản xuất, cũng như các thuốc chưa được MSD nhượng quyền, để xem xét việc cấp giấy đăng ký lưu hành thuốc. Do vậy, việc sử dụng thuốc molnupiravir hiện nay tại Việt Nam được tiến hành thông qua hình thức nghiên cứu tại cộng đồng trong khuôn khổ Chương trình thí điểm điều trị có kiểm soát chặt chẽ.
"Do thuốc chưa được cấp phép lưu hành rộng rãi nên việc quản lý thuốc nghiên cứu cần phải hết sức chặt chẽ để tránh thất thoát hoặc sử dụng sai mục đích nghiên cứu", theo đại diện Bộ Y tế.
Về nguyên tắc điều trị đối với thuốc kháng virus hiện tại ở Việt Nam, đối với thuốc chưa được Tổ chức Y tế Thế giới (WHO) khuyến cáo sử dụng, chưa được cấp phép lưu hành, sử dụng khẩn cấp tại bất kỳ nước nào, việc sử dụng phải tuân thủ các quy định về thử nghiệm lâm sàng của Bộ Y tế. Thuốc đã được WHO khuyến cáo sử dụng hoặc được cấp phép lưu hành, cấp phép sử dụng khẩn cấp tại ít nhất một nước, thì có thể được chỉ định điều trị theo diễn biến bệnh lý của người bệnh (ví dụ thuốc remdesivir, favipiravir...).
Bộ Y tế cho biết sẽ tiếp tục cập nhật các thông tin khoa học của thuốc cũng như tình hình cấp phép sử dụng tại các quốc gia, làm cơ sở báo cáo Chính phủ và các cơ quan chức năng cho phép cấp phép sử dụng khẩn cấp tại Việt Nam trong thời gian sớm nhất.
Molnupiravir cùng với favipiravir, remdesivir là 3 loại thuốc kháng virus đã được Bộ Y tế đưa vào phác đồ điều trị Covid-19 ở Việt Nam. Molnupiravir và favipiravir là hai loại thuốc kháng virus dạng viên, dùng theo đường uống, dễ dàng cho F0 điều trị tại nhà. Đây là lợi thế của hai loại thuốc này. Trong khi đó remdesivir là thuốc tiêm bắp, dùng cho bệnh nhân nặng, nên chỉ sử dụng trong bệnh viện.
Mới đây, Bộ Y tế công bố kết quả thử nghiệm molnupiravir, ghi nhận gần 100% bệnh nhân dùng thuốc có tải lượng virus thấp, tỷ lệ chuyển nặng rất thấp, không có ca tử vong.
Y học - Sức khỏe
-

Tại sao trứng gà tây không phổ biến trên bàn ăn?
-

Việt Nam có một loại củ phơi khô được ví như "thuốc trường thọ"
-

Những bức ảnh thay đổi cái nhìn về lịch sử
-

Vật nguy hiểm nhất thế giới: Chỉ nhìn 5 phút đã mất mạng, hàng trăm năm nữa cũng không thể đến gần!
-

Tại sao bạn dễ ngủ trên ghế sofa và sau đó tỉnh táo trên giường?
-

Dấu hiệu biển nước khổng lồ tồn tại dưới lớp vỏ Trái đất